通过H₂驱动温室气体CO₂转化为燃料和化学品,是缓解能源危机与气候问题的重要路径之一。产乙酸菌能够通过伍德-永达尔途径固定CO₂,并偶联能量代谢,实现自养生长。细胞固碳和ATP合成过程需要H₂等还原剂氧化产生的还原当量驱动。氢化酶能够催化H₂氧化、启动还原力生成,是影响细胞生长与CO₂固定效率的关键酶。
近日,中国科学院青岛生物能源与过程研究所一碳生物技术研究中心通过前期开发的CRISPR/Cas9基因编辑技术(Appl Environ Microbiol., 2025, 91(4):e0218324),敲除了模式产乙酸菌永达尔梭菌(Clostridium ljungdahlii)中被认为是“核心”的电子歧化氢化酶,意外发现菌株不仅未出现生长缺陷,反而实现了生物量、乙酸和乙醇产量的全面提升。通过热力学分析,其敲除启动了单亚基氢化酶的代偿功能,从而使氢气氧化从经典的电子歧化路线转换为铁氧还蛋白直接还原路线,新路线能量转换效率更高,从而提高了细胞的能量和还原力供给的。突变株在单细胞蛋白生产和还原性产物合成方面表现出一定的应用潜力。
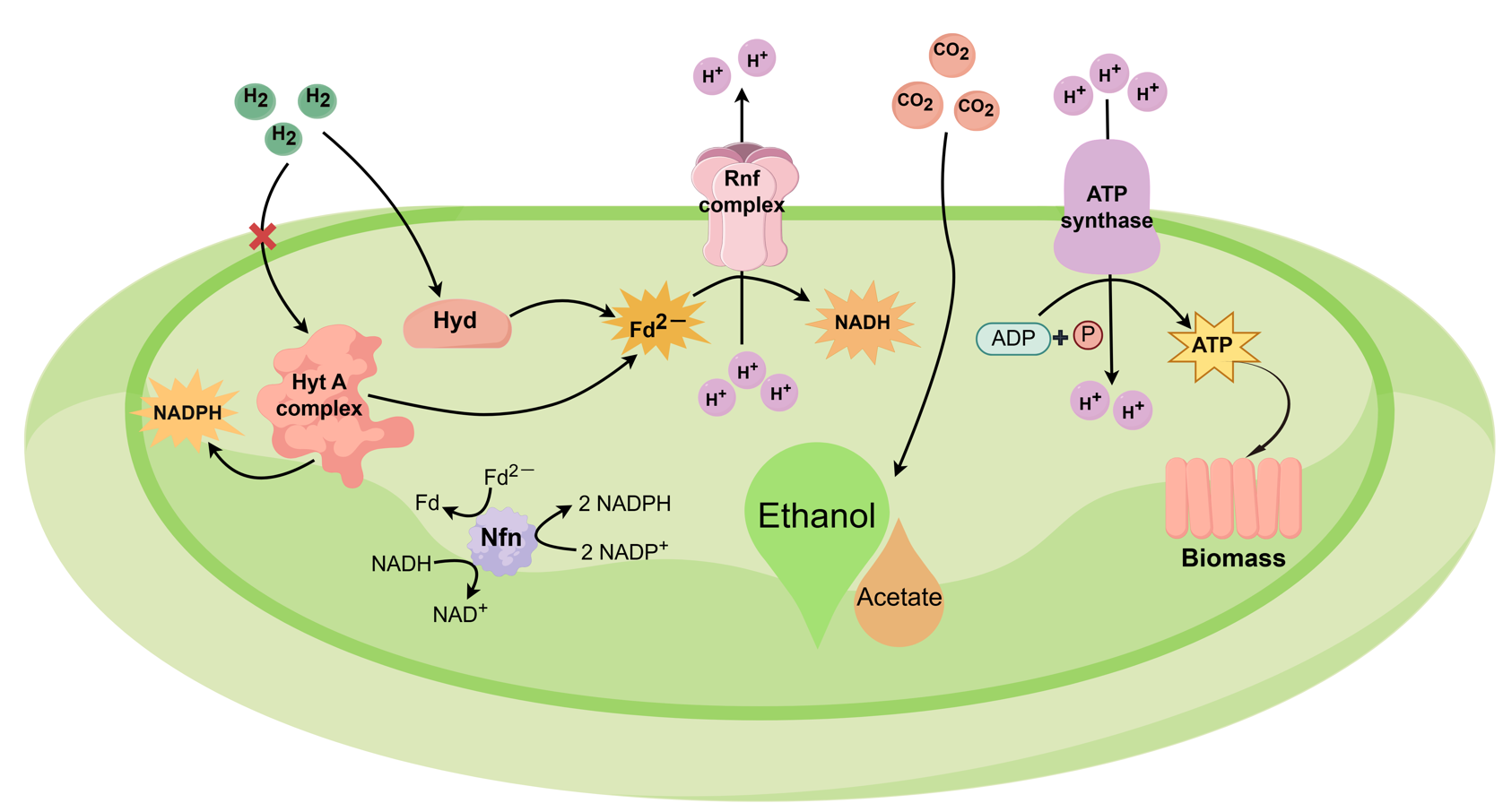
该研究表明,通过敲除特定基因解除细胞的“进化约束”,可为产乙酸菌的代谢工程改造提供可行策略。研究成果发表于《Bioresource Technology》,博士研究生文志琼和李煜真为论文共同第一作者,李福利研究员和马小清副研究员为共同通讯作者。该研究获得了国家重点研发计划、国家自然科学基金等项目的支持。(文/图 马小清)
原文链接:https://doi.org/10.1016/j.biortech.2026.134636
Zhi-Qiong Wen1, Yu-Zhen Li1, Hai-Jia Su, Jun-Zhe Zhang, Zi-Yong Liu, Shu-Ning Wang, Hui Wang, Fu-Li Li*, Xiao-Qing Ma*. Deletion of electron-bifurcating [FeFe]-hydrogenase enhances H₂-driven CO₂ fixation and ethanol production in Clostridium ljungdahlii. Bioresource Technology, 2026, 453: 134636